Pengukuran kalor sering dilakukan untuk menentukan kalor jenis suatu zat. Dengan mengetahui kalor jenis suatu zat maka dapat dihitung banyaknya kalor yang dilepaskan atau diserap dengan mengetahui massa zat dan perubahan suhunya, menggunakan persamaan Qdilepaskan = Qdiserap. Alat yang dapat digunakan untuk mengukur kalor adalah kalorimeter. Salah satu bentuk kalorimeter ialah kalorimeter campuran yang secara bagan tampak pada Gambar 1.3.3 . Kalorimeter terdiri atas komponen-komponen sebagai berikut.
- Sebuah bejana kecil terbuat dari logam tipis yang di gosok mengkilat. Bejana inilah yang dinamakan kalorimeternya.
- Sebuah bejana yang agak besar, untuk memasukkan kalorimeternya. Di antara kedua bejana itu dipasang isolator yang berfungsi untuk mengurangi kehilangan kalor karena dihantarkan atau dipancarkan sekitarnya.
- Penutup dari isolator panas yang telah dilengkapi dengan termometer dan pengaduk. Pengaduk biasanya juga terbuat dari logam sejenis.
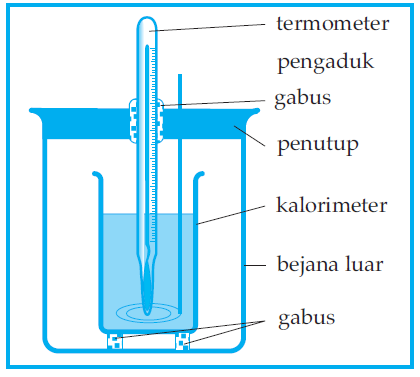
Gambar 1.3.3 kalorimeter
Pengukuran kalor berkaitan dengan banyaknya energi yang pindah. Pengukuran kalor sering dilakukan untuk menentukan kalor jenis suatu zat. Bila kalor jenis suatu zat diketahui, maka kalor yang diserap atau dilepaskan dapat ditentukan dengan mengukur perubahan suhu zat itu. Salah satu cara yang dapat digunakan ialah cara yang disebut : cara mencampurkan. Cara ini didasarkan atas suatu azas yang menyatakan bahwa bila dua zat yang suhunya berlainan dipersentuhkan (kontak termal), pada akhirnya suhu kedua zat itu akan menjadi sama. Alat yang dipergunakan untuk mengukur pertukaran kalor antara zat-zat yang dicampur adalah kalorimeter (Gambar 1.3.5).
Umumnya kalorimeter dimanfaatkan untuk menentukan kalor jenis suatu zat. Bila kalor jenis salah sau zat diketahui, maka kalor jenis zat yang lain dapat dihitung melalui penggunaan hukum kekekalan energi untuk kalor yang dirumuskan seperti persamaan (1.3.5). Dalam menentukan kalor jenis suatu logam secara eksperimen dengan metode mencampur, logam sampel yang massanya diketahui yang telah dipanaskan sampai suhu tertentu dicemplungkan ke dalam air yang suhunya lebih rendah. Setelah tercapai kesetimbangan, maka suhu campuran akan berada berada di bawah suhu logam, tetapi di atas suhu air. Dalam keadaan demikian, air di dalam kalorimeter dikatakan memperoleh kalor, sedangkan logam dikatakan melepas kalor. Kenyataan ini dinyatakan dengan persamaan:
Qlepas = Qterima
Mc (t1 – t2) = (m + m1c1)(t2 – t3) (1.3.6)
dengan M = massa logam (gram), c = kalor jenis logam sampel, t1 = suhu logam sebelum mencapai kesetimbangan, t2 = Suhu awal air dan kalorimeter, m = massa air, m1 = massa cawan kalorimeter, dan c = kalor jenis bahan pembuat cawan.
